Diagnostika ICHS
Podle Bayesova teorému je optimální indikovat neinvazivní vyšetření pro detekci ICHS u pacientů se střední předtestovou pravděpodobností ICHS(6,22). Pacienti s vysokou předtestovou pravděpodobností (např. muži s typickou anginou pectoris) mají být z diagnostických důvodů odesláni přímo na koronarografii, jelikož i při negativním nálezu neinvazivního vyšetření je riziko ICHS stále významné (neinvazivní vyšetření však může být cenné např. při rozhodování o revaskularizaci, pro detekci viability apod.)(6). Předtestová pravděpodobnost ICHS podle věku, pohlaví a typu obtíží je uvedena v tabulce 5.
Tabulka 5. Předtestová pravděpodobnost ICHS (%) podle věku, pohlaví a charakteru bolesti na hrudi.
Nejčastějším kritériem pro ověření přesnosti zátěžového testu je koronarografický nález a jako pozitivní pro ICHS bývá ve většině prací uváděno zúžení lumen jedné z hlavních epikardiálních tepen o 50 % a více, část prací si stanovuje jako kritérium 70 % zúžení.
Jak prokázali Van Train a spol.(23), volba 70 % nebo 50 % stenózy jako kriteria pro ICHS nemá signifikantní vliv na senzitivitu SPECT. Je však třeba se zmínit o tzv. potestové selekci - na koronarografii vždy směřují převážně pacienti s pozitivním nálezem při neinvazivním vyšetření.
Proto mají všechny soubory relativně nižší zastoupení koronarograficky ověřených osob s normálním nálezem, což může vést k ovlivnění výpočtu specificity. Při porovnávání neinvazivního vyšetření s koronarografií tedy můžeme narazit na určité obtíže a ani koronarografie není "zlatým standardem" - může význam stenózy podhodnocovat i nadhodnocovat, jak prokázaly práce s intravaskulární sonografií(24).
Navzdory těmto limitacím je koronarografické ověření výsledků neinvazivního vyšetření praktickým standardem. Skýtá možnost objektivně posoudit výsledky různých neinvazivních vyšetření (zátěžové EKG, dobutaminové echokardiografie a SPECT myokardiální perfuze). Další výhodou tohoto porovnávání je, že výsledek koronarografie je nejdůležitější pro další léčbu - konzervativní postup nebo perkutánní koronární intervence (PCI) resp. chirurgické řešení (CABG). V tabulce 6 je uveden přehled souborů pacientů, u nichž byla dg. přesnost SPECT ověřena koronarograficky.
Tabulka 6. Senzitivita, specificita a dg. přesnost zátěžového SPECT vyšetření myokardiální perfuze pro detekci ICHS.
Odkaz | | Senzitivita | | | Tamaki a spol.(2) | | | | | Mahmarian a spol.(3) | | | | | DePasquale a spol.(4) | | | | | Kamínek a spol.(26) | | | | | Casanova a spol.(27) | | | | | Santana-Boado a spol.(28) | | | | | Azzareli a spol.(29) | | | | | Iskandrian a spol.(30) | | | | | Lisbona a spol.(31) | | | | | Francisco a spol.(32) | | | | | Huikuri a spol.(33) | | | | | Nguyen a spol.(34) | | | | | Souhrnně | | | | |
Stratifikace rizika a posouzení závažnosti stenózy zjištěné při koronarografii
Hlavní výhoda SPECT vyšetření myokardiální perfuze vůči ostatním v současnosti rutinně prováděným zobrazovacím vyšetřením (tedy zejména zátěžové echokardiografii) spočívá v možnosti kvantitativního posouzení regionálních perfuzních abnormalit. Pacienti s normální perfuzí po adekvátní zátěži mají velmi nízkou frekvenci kardiálních příhod nezávisle na přítomnosti koronarograficky prokázané ICHS. Studie s více než 10 000 pacienty prokázaly, že riziko infarktu myokardu nebo náhlé srdeční smrti je u takových osob menší než 1% ročně(5,35,36). Dobrá prognóza se pojí i s nevelkým fixním defektem při celkově dobré funkci levé komory. Naopak riziko kardiální příhody lze předpokládat u všech pacientů s reverzibilním defektem perfuze. Vyšší riziko mají pacienti s rozsáhlým perfuzním defektem a při známkách pozátěžové dysfunkce LK (tranzientní ischemická dilatace LK, pokles pozátěžové EF, zvýšené vychytávání Tl-201 v plících).
a) Kvantitativní perfuzní SPECT
Pokud pomocí SPECT zobrazíme perfuzní defekty, nestačí popsat pouze jejich lokalizaci a zda se jedná o reverzibilní či fixní poruchu perfuze. Je nutné se vyjádřit také k rozsahu a závažnosti perfuzní abnormality. Tu lze kvantifikovat na polárních mapách pomocí segmentálního skóring systému (Obrázek 8)(37). Perfuze v jednotlivých segmentech je charakterizována zpravidla pětistupoovou škálou (0 - normální perfuze, 1 - nejednoznačný nález, 2 - abnormální perfuze, 3 - závažná porucha, 4 - absence vychytávání radiofarmaka). Každý ze segmentů LK je takto ohodnocen a body se sčítají - stanovuje se tzv. sumační zátěžové skóre (summed stress score, SSS) a sumační klidové skóre (summed rest score, SRS)(35,36). V současných nukleárně kardiologických vyhodnocovacích programech probíhá tato kvantitativní analýza plně automaticky podle počtu standardních odchylek ve srovnání s normálovou databází. Pokud je SSS menší než 4, je perfuzní defekt hodnocen jako nevýznamný. Naopak při SSS > 13 se jedná o těžkou poruchu perfuze a riziko je vysoké (Obrázek 9).
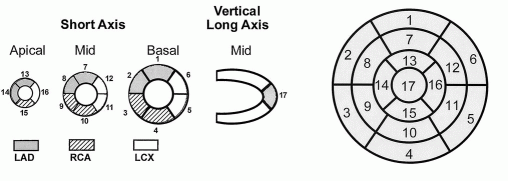 |
| Obrázek 8. Segmentální dělení tomografických řezů levé komory, tvorba polární mapy a povodí jednotlivých koronárních tepen.LAD = left anterior descending artery (ramus interventricularis anterior), LCX = left circumflex artery (ramus circumflexus), RCA = right coronary artery (arteria coronaria dextra). |
| [ Zvětšit obrázek na 100% originální velikosti ] |
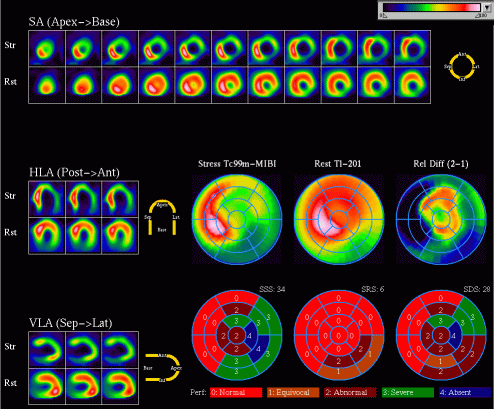 |
| Obrázek 9. Zátěž MIBI/klid 201Tl SPECT u 66leté pacientky prokazuje reverzibilní defekt perfuze anteriorně, apikálně, inferiorně a laterálně. Sumační zátěžové skóre (SSS) je 34, zatímco sumační klidové skóre (SRS) je 6. Koronarograficky bylo prokázáno závažné postižení všech tří tepen. |
| [ Zvětšit obrázek na 100% originální velikosti ] |
Hachamovitch a spol.(36) analyzovali soubor 5183 pacientů, kteří byli vyšetřeni pomocí SPECT myokardu. Zatímco u pacientů se sumačním zátěžovým skóre < 4 bylo riziko náhlé srdeční smrti nízké (0,3% ročně), u pacientů se sumačním zátěžovým skóre > 13 bylo evidováno 3,7% úmrtí ročně (tabulka 7). U pacientů s mírně abnormální perfuzí (SSS 4 - 8) je středně vysoké riziko infarktu myokardu, ale riziko srdeční smrti je nízké (Obrázek 10). U těchto pacientů by měla být preferována agresivní modifikace rizikových faktorů (sekundární prevence). U pacientů se střední a s těžkou abnormalitou perfuze (SSS > 8) je preferována invazivní strategie.
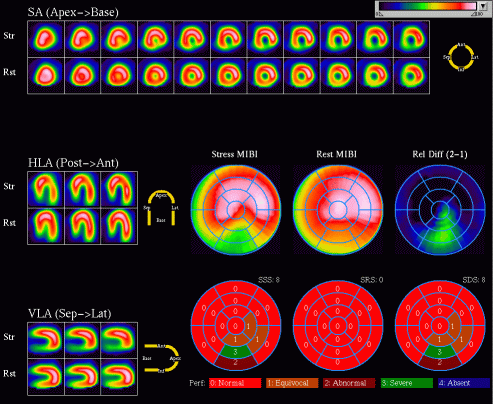 |
| Obrázek 10. Zátěžové MIBI SPECT vyšetření u 35letého pacienta s typickou anginou pectoris. Je zobrazen reverzibilní defekt inferiorně. Sumační zátěžové skóre (SSS) je 8, zatímco sumační klidové skóre (SRS) je 0. Koronarograficky po 4 týdnech prokázán 100% uzávěr ve středním úseku pravé koronární tepny, která se dále plní z povodí ramus interventricularis anterior. Pacientovy obtíže byly zvládnuty medikamentózně. |
| [ Zvětšit obrázek na 100% originální velikosti ] |
Tabulka 7. Frekvence náhlé srdeční smrti a nefatálního infarktu myokardu (% za rok) u 5183 pacientů vyšetřených pomocí SPECT myokardiální perfuze podle závažnosti poruchy perfuze. SSS - summed stress score (sumační zátěžové skóre), n - počet pacientů. Frekvence kardiální příhody se signifikantně zvyšuje s rostoucím SSS.(36)
Zátěžová perfuze | | | Nefatální infarkt myokardu | Normální (n=2946) | | | | Mírně abnormální (n=884) | | | | Středně abnormální (n=455) | | | | Těžká porucha (n=898) | | | |
b) Gated SPECT a stratifikace rizika
Hachamovitch a spol.(38) sledovali soubor 1695 osob a prokázali, že pacienty s abnormálním sumačním zátěžovým skóre (SSS) lze dále třídit podle výsledku gated SPECT. Mortalita byla signifikantně vyšší u pacientů s nízkou pozátěžovou EF.
Obdobně Sharir a spol.(39) v souboru 1680 pacientů prokázali vyšší riziko u osob s pozátěžovou EF < 45 % a se zvýšeným end-diastolickým objemem (> 120 ml) resp. end-systolickým objemem (> 70 ml).
I když zátěžové SPECT vyšetření myokardialní perfuze s vysokou dg. přesností identifikuje pacienty s ICHS, u pacientů s nemocí více tepen nemusí být zobrazen perfuzní defekt ve všech postižených povodích(25). Metoda totiž posuzuje spíše relativní než absolutní perfuzi, v některých případech dochází k přerušení zátěže pro symptomy anginy pectoris při ischemii vyvolané v nejvíce postiženém povodí.
Novější práce ukázaly, že tyto rizikové pacienty se závažným postižením koronárního řečiště pomáhá identifikovat poischemické omráčení LK zjištěné pomocí gated SPECT (40-43). často je zjištěn významný pokles pozátěžové EFLK ve srovnání s klidovou hodnotou nebo regionální zhoršení kinetiky LK
(Obrázek 11a, Obrázek 11b, Obrázek 11c).
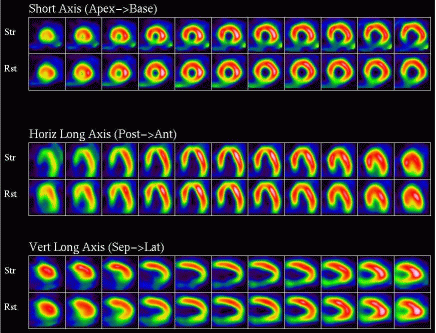 |
| Obrázek 11. 61letý pacient byl odeslán na zátěžové MIBI SPECT vyšetření pro námahovou bolest na hrudi a abnormální klidové EKG (RBBB). (A) Na tomografických řezech je zobrazen závažný reverzibilní defekt perfuze inferoseptálně. |
| [ Zvětšit obrázek na 100% originální velikosti ] |
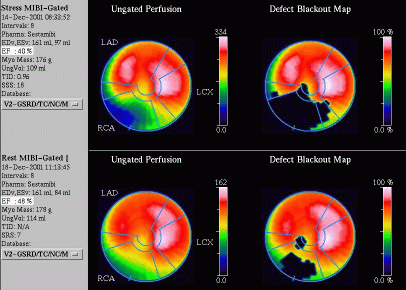 |
| Obrázek 11. 61letý pacient byl odeslán na zátěžové MIBI SPECT vyšetření pro námahovou bolest na hrudi a abnormální klidové EKG (RBBB). (B) Na polárních mapách je defekt lokalizován do povodí pravé koronární tepny. Sumační zátěžové skóre (SSS) je 18, zatímco sumační klidové skóre (SRS) je 7. |
| [ Zvětšit obrázek na 100% originální velikosti ] |
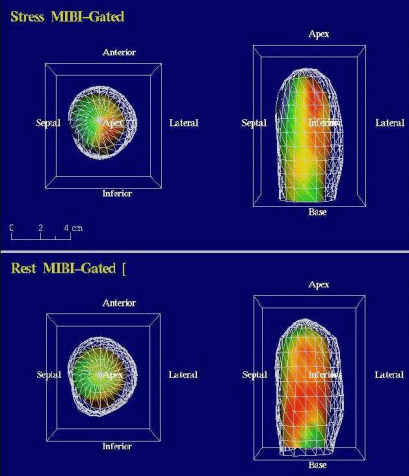 |
| Obrázek 11. 61letý pacient byl odeslán na zátěžové MIBI SPECT vyšetření pro námahovou bolest na hrudi a abnormální klidové EKG (RBBB). (C) Gated SPECT 3D obrazy ukazují poischemické omráčení, pozátěžová EF je snížena na 40%, zatímco klidová EF je 48%. Následně provedená koronarografie odhalila 70% stenózu ramus interventricularis anterior za odstupem normální jediné diagonální větve, 75% stenózu ramus circumflexus a 100% uzávěr v proximálním úseku pravé koronární tepny. |
| [ Zvětšit obrázek na 100% originální velikosti ] |
Toto omráčení (stunning) může trvat až 1 hod po zátěži, a lze je proto prokázat v době akvizice pozátěžové gated SPECT studie(44,45). Předpokládá se, že repetitivní stunning může vést postupně k chronické depresi funkce levé komory (hibernaci nebo i k ireverzibilnímu poškození)
(Obrázek 12a, Animace 2, Obrázek 12b, Animace 3).
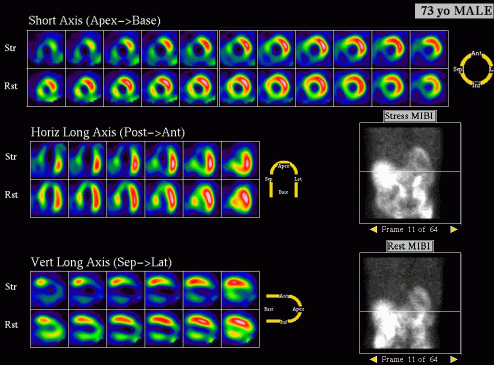 |
| Obrázek 12. 73letý muž, odeslaný k detekci ICHS pro narůstající atypické obtíže při námaze (dušnost). Na tomografických řezech (A) i na polárních mapách (B) je zobrazen rozsáhlý zátěží navozený parciálně reverzibilní defekt perfuze. Zátěž byla provedena dipyridamolem, po 1. min. infuze byla přerušena pro bolest na hrudi. po infuzi dipyridamolu výrazný pokles pozátěžové gated SPECT EF na 24%. Druhý den po zátěžovém testu bylo provedeno klidové vyšetření, kdy funkce byla upravena jen částečně - EF 45% (AVI 2, AVI 3). Avšak dle echokardiografie měl pacient před vyšetřením normální systolickou funkci a EF byla 60%. Koronarograficky bylo prokázána 70% stenóza kmene levé věnčité tepny a výrazné difuzní postižení koronárního řečiště a byl indikováno urgentní chirurgické řešení. |
| [ Zvětšit obrázek na 100% originální velikosti ] |
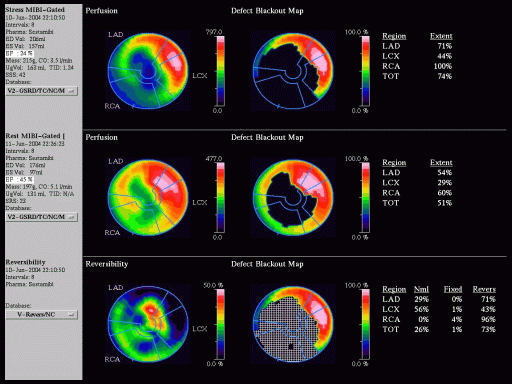 |
| Obrázek 12. 73letý muž, odeslaný k detekci ICHS pro narůstající atypické obtíže při námaze (dušnost). Na tomografických řezech (A) i na polárních mapách (B) je zobrazen rozsáhlý zátěží navozený parciálně reverzibilní defekt perfuze. Zátěž byla provedena dipyridamolem, po 1. min. infuze byla přerušena pro bolest na hrudi. po infuzi dipyridamolu výrazný pokles pozátěžové gated SPECT EF na 24%. Druhý den po zátěžovém testu bylo provedeno klidové vyšetření, kdy funkce byla upravena jen částečně - EF 45% (AVI 2, AVI 3). Avšak dle echokardiografie měl pacient před vyšetřením normální systolickou funkci a EF byla 60%. Koronarograficky bylo prokázána 70% stenóza kmene levé věnčité tepny a výrazné difuzní postižení koronárního řečiště a byl indikováno urgentní chirurgické řešení. |
| [ Zvětšit obrázek na 100% originální velikosti ] |
Vyšetřování pacientů po revaskularizaci
U pacientů po PCI nebo CABG je indikována zátěžová scintigrafie myokardu zejména při rekurenci symptomů. Rutinní vyšetřování všech asymptomatických osob po revaskularizaci není zahrnuto v doporučených postupech. Indikace SPECT myokardu je oprávněná u pacientů s pozitivní či nediagnostickou zátěžovou elektrokardiografií. Klinický prospěch z neinvazivního zobrazovacího vyšetření mohou mít rovněž asymptomatičtí diabetičtí pacienti, stejně jako pacienti více než 5 let po CABG (zvláště mají-li venózní štěpy), a pacienti s inkompletní revaskularizací(10). Díky obrovskému rozvoji intervenční kardiologie v posledních 10 letech tvoří v současnosti porevaskularizační studie velmi významný a neustále narůstající podíl v zastoupení jednotlivých indikací SPECT vyšetření(46).
Detekce viability
Zjištění viability myokardu má klinický význam u pacientů s dysfunkcí levé komory a nízkou EF levé komory (EF pod 40%)(6). Signifikantně horší prognózu mají nemocní s dysfunkčním viabilním myokardem, nejsou-li revaskularizováni, než ti, kteří se podrobili revaskularizaci, nebo než nemocní s dysfunkčním neviabilním myokardem(6,47). Zátěžové vyšetření myokardiální perfuze umožouje detekovat ischemii i viabilitu. Pokud je klinický dotaz pouze na viabilitu nebo pacient není schopen zátěže, lze provést pouze klidové vyšetření. Dysfunkční segmenty s fixním defektem kumulujícím méně než 50 % maximální aktivity (četnosti impulsů) jsou obvykle považovány za jizvu po infarktu myokardu, zatímco kumulace větší než 50 % maxima svědčí pro hibernující myokard(16). Klinický přínos má u vybraných pacientů rovněž vyšetřování metabolizmu glukózy pomocí F-18-fluorodeoxyglukózy (FDG). Ischemický, ale viabilní myokard je charakterizován sníženou perfuzí se současně zachovanou nebo dokonce vyšší akumulací FDG (tzv. "perfuzně-metabolický mismatch"). Vyšetření pomocí FDG je považováno za "zlatý standard" pro detekci viability, u většiny pacientů lze však viabilitu detekovat pomocí SPECT po aplikaci Tl-201 nebo Tc-99m značených radiofarmak nebo dobutaminovou echokardiografií(16,47). FDG vyšetření je indikováno u pacientů s nediagnostickým závěrem těchto standardních vyšetření.
Akutní koronární syndrom
U pacientů přijatých na koronární jednotku pro bolesti na hrudi byl prokázán přínos vyšetření pomocí 99mTc-MIBI (resp. tetrofosmin) SPECT u nerozhodnutých stavů (bez elevace ST úseku na EKG a bez pozitivity kardioselektivních enzymů). Namísto další observace je pacient při nálezu normální perfuze propuštěn domů a dochází tak k výrazné úspoře prostředků. Limitací je však zejména 24 hod. dostupnost SPECT, a metodu tudíž provádí rutinně jen několika evropských center (poněkud více je rozšířena v USA)(48).
Srovnání SPECT a zátěžové echokardiografie
Komparativní analýzu těchto neinvazivních vyšetření provedli Gerson a Hoit(49). Každá z těchto metod má svoje výhody i nevýhody. Obě metody umožoují s vysokou diagnostickou přesností detekovat ICHS. Lehce vyšší senzitivitu vykazuje SPECT, vyšší specificitu naopak zátěžová echokardiografie, signifikantní rozdíly při detekci ICHS však nebyly prokázány. Výhodou echokardiografie je nižší cena a absence ionizujícho záření, vyžaduje však značné zkušenosti vyšetřujícího personálu. Jelikož SPECT zobrazuje přímo myokardiální perfuzi, a to trojrozměrně, umožouje přesnější lokalizaci defektu. Vyšetření má vynikající reprodukovatelnost, pomocí nových nukleárně kardiologických softwarů lze automaticky kvantifikovat rozsah a závažnost perfuzních abnormalit. SPECT se proto jeví výhodnější při stratifikaci rizika u pacientů se známou nebo suspektní ICHS a při vyšetřování pacientů po PCI nebo CABG. Pro detekci viability nebyly zjištěny signifikantní rozdíly mezi SPECT a dobutaminovou echokardiografií. V některých situacích může být výhodné obě metody kombinovat(50,51).
Limitace metod
SPECT myokardiální perfuze je vysoce senzitivním testem pro detekci ICHS, přičemž zobrazení perfuzních abnormalit je častější u pacientů s nemocí více tepen než u pacientů s nemocí jedné tepny(23,25). Jistou limitací SPECT je, že zobrazuje spíše relativní než absolutní myokardiální perfuzi. Pokud tedy je snížený průtok ve všech třech povodích, jako normální se na SPECT zobrazuje povodí s nejlepším průtokem (tedy s nejmenším postižením). Navíc, pokud je při zátěžovém testu indukována ischemie související s nejvýznamnější stenózou koronárního řečiště, ischemické symptomy mohou zabránit v dalším pokračování zátěže, a nedojde tak k zobrazení dalších perfuzních defektů.
V multicentrické studii Van Traina a spol.(23) byla senzitivita SPECT pro detekci ICHS u pacientů s nemocí 1, 2 a 3 tepen 84 %, 91 % resp. 96 %. Avšak správná identifikace rozsahu onemocnění byla u pacientů s postižením 2 a 3 tepen pouze 43 % resp. 38 %. V našem souboru 151 pacientů kvantitativní analýza perfuze ukázala narůst sumačního zátěžového skóre se stoupajícím počtem postižených povodí: průměrné SSS bylo 9 pro nemoc 1 tepny, zatímco při postižení 2 a 3 povodí bylo SSS 15 resp. 16(52). Avšak pouze 48 % (30/63) pacientů s nemocí více tepen mělo reverzibilní defekty ve více povodích. Může tak docházet k určitému podhodnocení u pacientů s nemocí více tepen, vybalancované postižení všech tří tepen dokonce může být vzácnou příčinou falešně negativního zátěžového SPECT vyšetření(53). Naštěstí má 96% pacientů s nemocí tří tepen abnormální perfuzní SPECT. Toto číslo je navíc možno zvýšit pomocí vedlejších ukazatelů, jako je tranzientní ischemická dilatace, pozátěžové zhoršení ejekční frakce levé komory a u thalliové scintigrafie vyšší kumulace radiofarmaka v plících.
|
